经过 20 年不懈的努力,科学家们终于实现了一个伟大的目标:成功地将成熟细胞转化成原始血细胞(可以自我更新)以及血液中其他细胞。这项研究成果刊登在 5 月 17 日的《自然》杂志上。
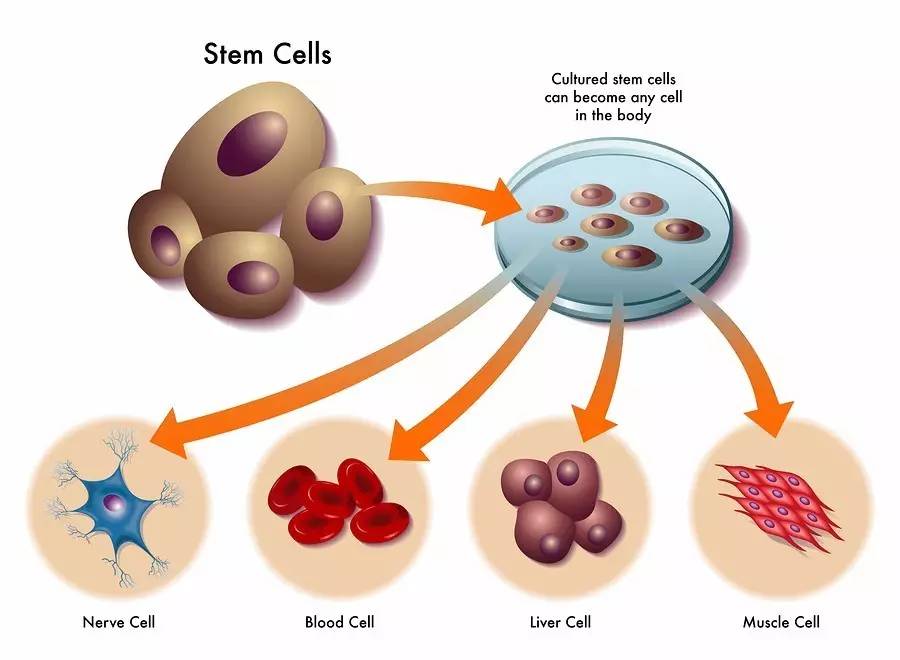
图丨干细胞可以培养成各类型人体细胞
这项成果为白血病或其他血液疾病的患者带来了新的希望。以往,这些患者通常需要进行骨髓移植,但寻找到可兼容供体者的概率却十分之小,导致很多人因此无法得到及时的治疗。
如果上述研究成果可以顺利转化为临床治疗方法,类似的悲剧就可以得到避免,因为患者们可以依靠自身健康细胞诱导出造血干细胞。
通常而言,造血干细胞产生于在胚胎发育期间,而成年人的造血干细胞存在于骨髓之中,并负责补充红细胞、白细胞和血小板的供应量。而当这些细胞不能正常工作时,血红细胞的供应就会受到影响。一旦没有足够的血液抵达身体组织,甚至影响到心脏等器官时,就会导致严重疾病。
可以说,大部分白血病都直接或间接与造血干细胞异常相关。
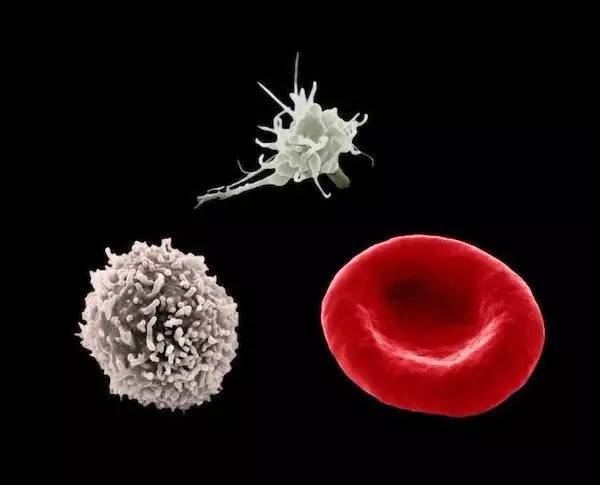
图丨红细胞(右)、白细胞(左)和血小板(上)
正常的造血干细胞具有长期自我更新的能力,以及分化成各类成熟血细胞的潜能。自 1998 年人的胚胎干细胞(ES)被成功分离出来,科学家们就一直在尝试着用它们去“制造”造血干细胞,但一直没能获得成功。
因此,此次研究成果意义重大,这得益于以下两个实验室的各自工作:
一、麻省波士顿儿童医院的团队;该团队由干细胞生物学家 George Daley 领导,他们创造了一种类似于血液干细胞,但又不同于人体细胞的干细胞。
二、纽约市威尔康乃尔医学院的团队;由干细胞生物学家 Shahin Rafii 领导,他们将小鼠体内的成熟细胞诱导成了完全成熟的造血干细胞。

图丨造血干细胞和祖细胞,它们是由研究人员通过诱导人类多能干细胞制备而来的
那么他们是如何实现的呢?
麻省波士顿儿童医院 George Daley 的团队选择将成人皮肤细胞和其他细胞作为原材料。他们先通过现有的方法将细胞重新编程,使其转变为诱导型多能干细胞(iPSC)——这种细胞能够分化产生其它类型的细胞。

图丨干细胞生物学家George Daley
接下来,该团队进行了非常有创造力的一步:将 7 个转录因子(能够控制其他基因表达的基因)插入到iPS细胞的基因组中,并将这些被修饰了的人细胞注射入小鼠体内中进行培养。
12 周后,研究团队迎来了一个令人欣喜的结果:iPS细胞已经转化成了造血干细胞,它可以产生人体血液中的各种血液细胞以及免疫细胞,而且这种细胞与人体中天然存在的造血干细胞“出奇得相似”。
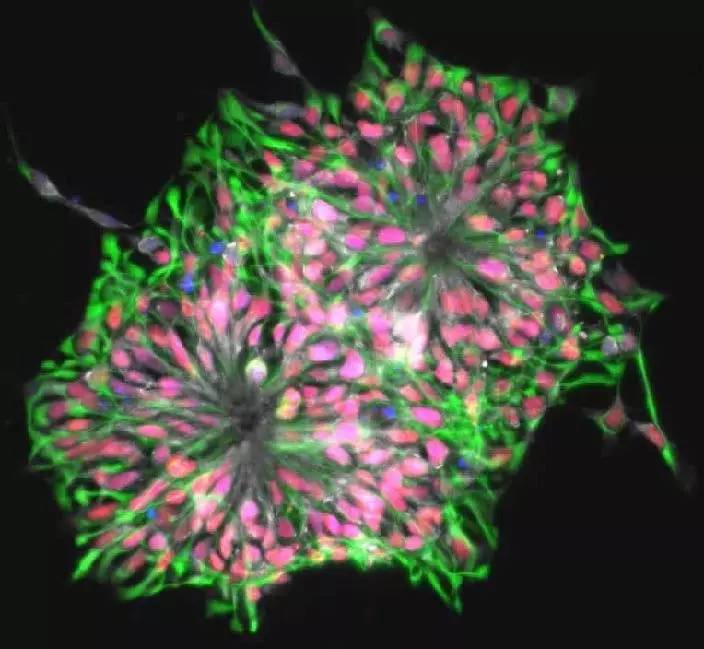
图丨诱导型多能干细胞
然而,以往的生物学认为,只有植物细胞,才能完成去分化和再分化过程,回到多能干细胞状态再分化成其他组织,而动物细胞只能不断继续分化的命运,直到终老。
直到 2006 年,这一曾经被写入教科书的生物学“常识” 被日本京都大学山中伸弥教授打破:他从 24 种与多能干细胞功能相关的转录因子中,找到四个对逆转已分化细胞充分必要的转录因子:Oct4,Sox2,cMyc和 Klf4,成功使它们去分化成多能干细胞。
这四个重编程因子后来被称为“山中因子”。2012年, 山中伸弥也因对iPSC 技术的贡献荣获诺贝尔医学奖。

图丨山中伸弥
iPSC技术从 2006 年发表以来一直备受瞩目,“山中因子”的经典配方也被后人持续更新,甚至发展出单纯小分子诱导版本。从临床角度,iPSC技术最大的优势就在于,可以避免使用伦理争议性较大的胚胎干细胞,一点皮肤,一点毛囊就可以转变成任意体细胞。
相比之下, 纽约市威尔康乃尔医学院 Shahin Rafii 的团队则是避开了诱导 iPS 细胞这个中间步骤,从小鼠中生产出真正的造血干细胞。他们的步骤如下:
一、研究人员首先从成熟小鼠的血管内层提取了细胞;
二、他们将四个转录因子插入到这些细胞的基因组中,接着用模拟人血管内环境的培养皿培养它们;
三、这些细胞转变成了血液干细胞并开始增殖。

图丨干细胞生物学家Shahin Rafii
当研究人员将这些干细胞注射到放疗后的小鼠(大部分血细胞和免疫细胞已被杀死)时,他们发现,小鼠可以从放疗损伤中恢复过来!这意味着,这些干细胞实现了血细胞再生(包括免疫细胞),小鼠因此可以继续存活,并且生存期超过了 1.5 年。

由于绕过了 iPS 细胞阶段, Shahin Rafii 将这种方法比作“直达月球的航班”,而将 George Daley 的方法比作为“先绕月球飞行后再抵达月球的航班”。也就是说,他认为自己的方法更加直接、省时和高效。
但是,George Daley 和其他研究人员相信,他们所使用的方法更有效,而且引起肿瘤生长和其他异常出现的概率更小。
图丨人体肿瘤
对此,加利福尼亚州拉霍亚斯克里普斯研究所的干细胞研究员 Janne Loring 在接受采访时表示,最佳的方法可能是仅仅去临时改变 iPS 细胞中的基因表达,而非永久性地插入具有编码转录因子的基因。
她指出,iPS 细胞容易从皮肤和其他组织中获取,而 Shahin Rafii 方法中的细胞却难以采集并在实验室培养。
无论如终,时间最终会证明哪种方法更适合实际情况。不过,这些进展已经足够鼓舞那些曾经感到希望渺茫的研究人员。此前,很多人已经对此不抱希望了,他们甚至认为,这些细胞在大自然中并不存在。事实证明,这种想法是错误的。